新规发布,疫苗杂质分析有难题?

图片来源:药监局官网
2023年10月12日,国家药监局、国家卫生健康委发布实施《中华人民共和国药典》(2020年版)第一增补本的公告。《公告》指出,《中华人民共和国药典》(2020年版)第一增补本,自2024年3月12日起施行。其中,在三部新增通则和指导原则中发布了“9403 人用疫苗杂质控制技术指导原则”,“人用疫苗杂质控制技术指导原则”公示稿曾于2021年9月在药典委官网发布。
该指导原则是对人用疫苗产品杂质控制的基本考虑,旨在指导疫苗生产和研发过程中对杂质成分的分析、评估并制定相应的控制策略,以尽可能减少或消除杂质对疫苗安全性和有效性的影响,保证疫苗产品质量。该指导原则应基于具体疫苗品种的特点及相关知识参考使用。指导原则主要分为三部分内容,分别为:
1)疫苗杂质来源。阐述了工艺相关杂质和产品相关杂质两大疫苗杂质来源,并提到要重点关注宿主细胞蛋白和核酸、所用生物/化学材料的残留物以及包材相容性研究。
2)疫苗杂质控制的原则及策略。疫苗杂质控制应基于“质量源于设计”的原则,对疫苗中杂质进行风险评估、全过程控制和全生命周期管理,并列举了不同类型疫苗杂质的控制要点(如下图所示)。同时在文中提到有机溶剂的使用应符合“残留溶剂测定法”(通则0861)以及参照“分析方法验证指导原则”(指导原则9101)对检测方法进行验证,并重点关注方法的专属性和灵敏度。

3)变更事项对疫苗杂质控制的影响。应定期评估上市疫苗的生产工艺性能和杂质控制策略的有效性,持续优化产品杂质控制策略,如发生变更应参照相关要求开展变更前后的可比性研究等。
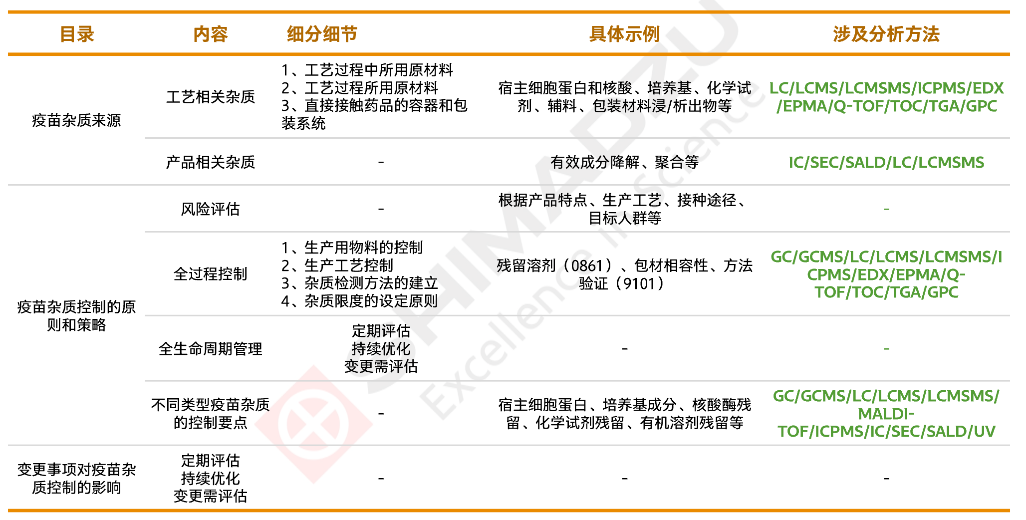
指导原则9403 全文可概括如下方表格所示:
疫苗接种每年可拯救数百万人的生命,其通过与身体的天然防御系统协同作用来建立保护网,从而降低感染疾病的风险。据统计迄今拥有的疫苗可以预防20多种危及生命的疾病,帮助所有年龄段的人活得更长、更健康。目前,疫苗接种每年可防止350万至500万人死于白喉、破伤风、百日咳、流感和麻疹等疾病。疫苗接种是初级卫生保健的一个关键组成部分,也是一项无可争议的人权。它也是钱能买到的最好的健康投资之一。疫苗对预防和控制传染病暴发至关重要,疫苗支撑着全球卫生安全,并将成为抗击抗微生物药物耐药性斗争的重要工具。(摘自WHO官网)
然而直到今天,全球疫苗安全事件仍层出不穷。不规范的管理、不合法的添加、不合规的质量控制都是疫苗安全事件频发的原因,进而导致疫苗这一本用于预防/治疗疾病的工具却成为了加速疾病和死亡的利器。在疫苗的质量控制中,杂质的分析和控制至关重要,疫苗中杂质种类繁杂,来源多样,同时在指导原则9403中强调了要重点关注分析方法的专属性和灵敏度,这使得杂质分析难度进一步提升。岛津于2017年起先后与权威机构和知名疫苗企业开展合作,有着非常丰富的经验和专业的团队,在本篇中小编将和您分享岛津的疫苗杂质分析方案,助力广大用户应对新规发布及实施。
01液相色谱法检测疫苗中四种常见防腐剂残留
● 分析条件
分析仪器:岛津超高效液相色谱仪LC-40
色谱柱:Shimadzu Shim-pack GIST 100 mm x 2.1 mm I.D., 2.0 μm; P/N: 227-3001-04; 岛津(上海)实验器材有限公司
流动相:A-水,B-乙腈
流速:0.4 mL/min
柱温:40 ℃
进样体积:5 μL
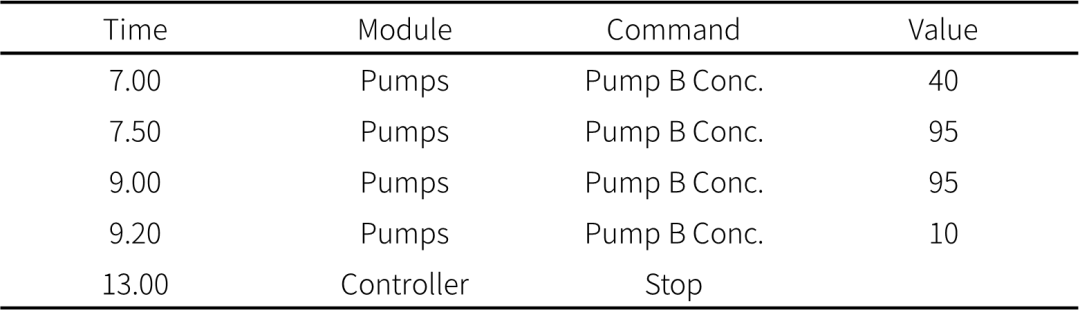
洗脱方式:梯度洗脱,B相初始浓度为10%。时间程序见表1。
表1:梯度洗脱时间程序
● 专属性及加标回收实验
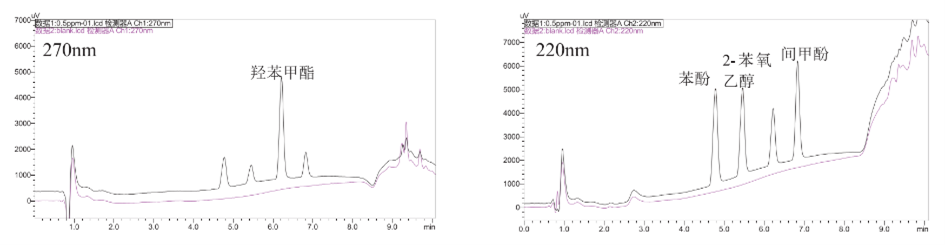
图1:对照品(0.5 ppm)和空白溶剂270 nm和220 nm色谱图
表2:样品加标回收率(n=3)
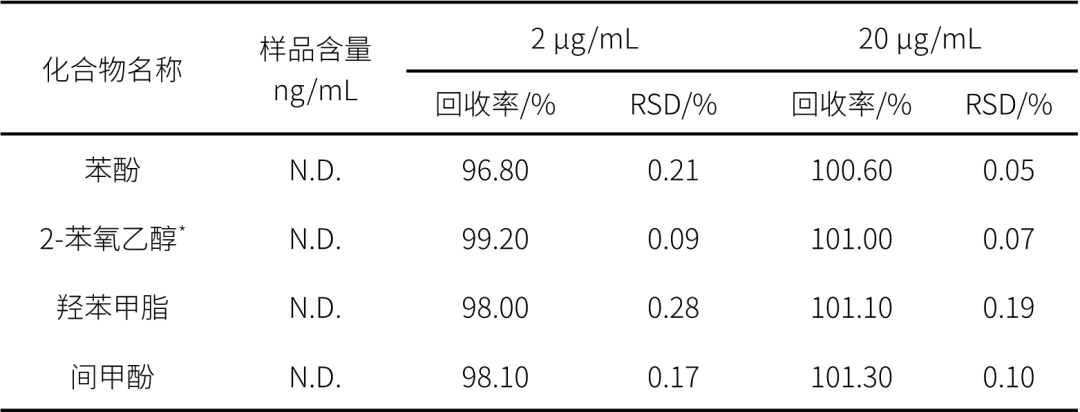
注:N.D.表示未检出
结果显示,方法专属性良好,符合9403要求,且加标回收率在96.8~101.30%之间,RSD在0.05~0.28%之间,方法可靠,可为疫苗中防腐剂残留分析提供参考。
02LCMSMS检测疫苗中卡那霉素残留
生物制品中卡那霉素的检测常用免疫法,但前处理复杂、灵敏度和专一性受限;LCMSMS方法前处理简单、专一性强、灵敏度高、分析速度快,因此本应用采用LCMSMS方法检测卡那霉素。
● 分析条件
分析仪器:岛津超高效液相色谱仪LC-40与三重四极杆质谱仪LCMS-8045联用系统
色谱柱:Shimadzu Shim-pack GIST Amide 150 mm x 2.1 mm I.D., 3.0 μm; P/N: 227-30818-06; 岛津(上海)实验器材有限公司
流动相:A-250 mM甲酸铵+0.1% 甲酸水溶液,B-乙腈
流速:0.8 mL/min
柱温:50 ℃
进样体积:10 μL
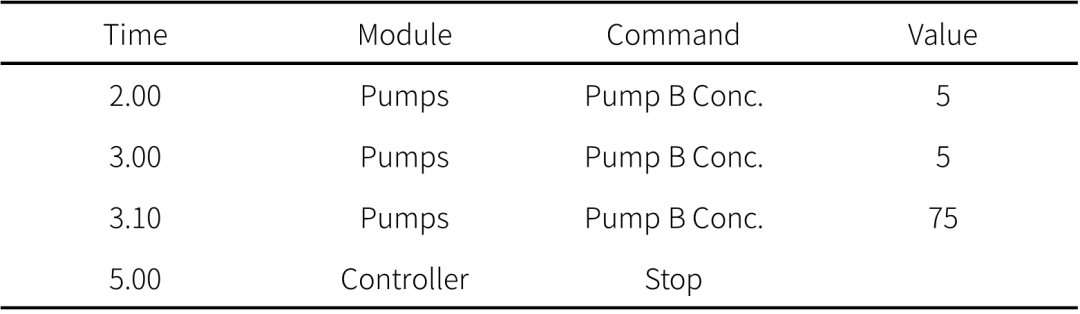
洗脱方式:梯度洗脱,B相初始浓度为75%。时间程序见表3。
表3:梯度洗脱时间程序
● 专属性及加标回收实验
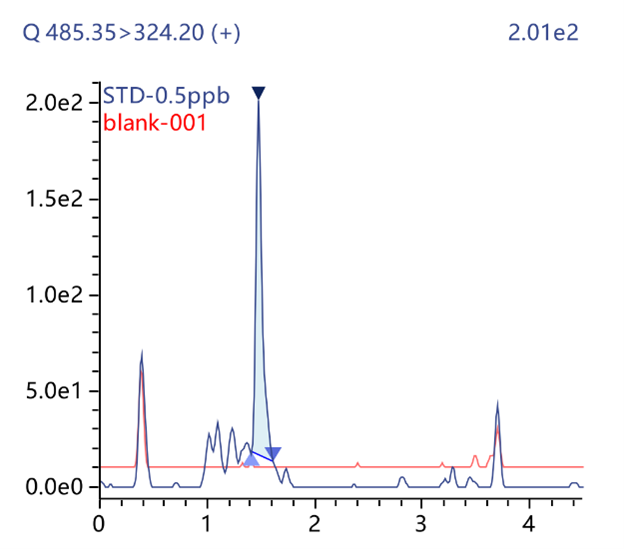
图2:对照品(0.5 ppm)和空白溶剂270 nm和220 nm色谱图
表4:样品加标回收率(n=3)
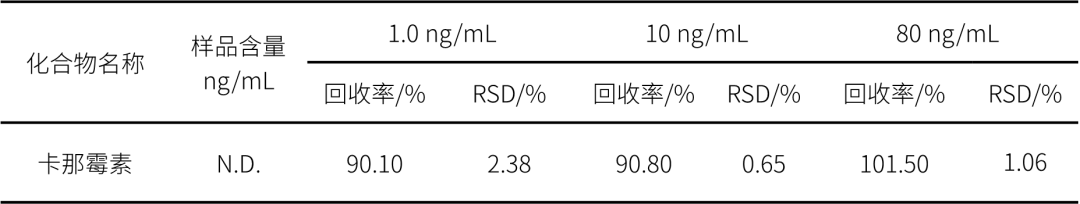
注:N.D.表示未检出
结果显示,方法专属性良好,符合9403要求,且加标回收率在90.10~101.50%之间,RSD在0.65~2.38%之间,方法可靠,可为疫苗中抗生素残留分析提供参考。
如果您想了解更多应用文章及细节,请扫描下方二维码下载

1 从生产到质量评价——疫苗行业整体解决方案
2 液相色谱法检测疫苗中四种常见防腐剂残留
3 LCMSMS检测疫苗中卡那霉素残留
4 ICPE-9820同时定量某疫苗中的铝佐剂和硫柳汞
5 Aggregates Sizer 在疫苗聚集体评价系统中的应用
岛津始终关注大家的用药安全,并积极应对法规要求和变化,更多第一增补本增修订应用方案将持续推出,敬请期待!

